Химические свойства этиленгликоля, характеристика. Двухатомный спирт. Эфиры этиленгликоля

Химические свойства этиленгликоля, характеристика. Двухатомный спирт. Эфиры этиленгликоля
Двухатомные спирты (гликоли)
По систематической номенклатуре названия двухатомных спиртов образуются от названия соответствующих алканов с прибавлением окончания «диол», положение -ОН групп указывается цифрами
По рациональной номенклатуре сохраняются названия от соответствующих алкенов с прибавлением слова «гликоль»
Способы получения гликолей
Двухатомные спирты можно получить теми же способами, что и одноатомные спирты, или другими.
Важнейшие из них – следующие:
2. Гипохлорирование алкенов:
3. Гидролиз окиси этилена:
4. Окисление алкенов.
Химические свойства
За счет взаимного влияния атомов подвижность водорода в гидроксильных группах этиленгликоля значительно больше, чем в спиртах. Гликоли обладают большими кислыми свойствами, чем спирты, и взаимодействуют не только с активными металлами, но и с гидроксидами металлов, образуюя комплексные структуры.
1. Взаимодействие с Cu(OH)2 (качественная реакция на гликоли):
2. Взаимодействие со спиртами:
При этом происходит образование моно- и дипроизводных.
3. Межмолекулярная дегидратация гликолей:
Нитроэфиры обладают взрывчатыми свойствами.
5. Гидрогалогенирование этиленгликоля:
Применение
Этиленгликоль – вязкая бесцветная жидкость, значительно уменьшает температуру замерзания воды и поэтому используется как антифриз, 60% водный раствор этиленгликоля замерзает при -50°С. Этиленгликоль применяется в органическом синтезе для получения полиэфиров, смол, волокна ловсан.
Применяется также при изготовлении печатных красок, нанесении рисунка на ткань.
93.79.221.197 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
Химические свойства этиленгликоля, характеристика. Двухатомный спирт. Эфиры этиленгликоля
Самые известные и применяемые в жизни человека и в промышленности вещества, принадлежащие к категории многоатомных спиртов – это этиленгликоль и глицерин. Их исследование и использование началось несколько веков назад, но свойства этих органических соединений во многом неповторимы и уникальны, что делает их незаменимыми и по сей день. Многоатомные спирты используют во многих химических синтезах, отраслях промышленности и сферах человеческой жизнедеятельности.
Первое «знакомство» с этиленгликолем и глицерином: история получения
В 1859 году, посредством двухстадийного процесса взаимодействия дибромэтана с ацетатом серебра и последующей обработки едким кали полученного в первой реакции этиленгликольдиацетата, Шарль Вюрц впервые синтезировал этиленгликоль. Некоторое время спустя был разработан метод прямого гидролиза дибромэтана, но в промышленных масштабах в начале двадцатого века двухатомный спирт 1,2-диоксиэтан, он же – моноэтиленгликоль, или просто гликоль, в США получали посредством гидролиза этиленхлоргидрина.
На сегодняшний день и в промышленности, и в лаборатории применяют ряд других методов, новых, более экономичных с сырьевой и энергетической точек зрения, и экологичных, так как применение реагентов, содержащих или выделяющих хлор, токсины, канцерогены и другие опасные для окружающей среды и человека вещества, сокращается по мере развития «зелёной» химии.
Аптекарем Карлом Вильгельмом Шееле в 1779 году был открыт глицерин, а особенности состава соединения изучил в 1836 году Теофиль Жуль Пелуз. Двумя десятилетиями позже было установлено и обосновано строение молекулы данного трёхатомного спирта в трудах Пьера Эжена Марселея Вертело и Шарля Вюрца. Наконец, ещё двадцать лет спустя Шарль Фридель провёл полный синтез глицерина. В настоящее время промышленность использует два метода его получения: через хлористый аллил из пропилена, а также через акролеин. Химические свойства этиленгиликоля, как и глицерина, широко используют в различных сферах химического производства.
Строение и структура соединения
В основе молекулы лежит непредельный углеводородный скелет этилена, состоящий из двух атомов карбона, в котором произошёл разрыв двойной связи. На освободившиеся валентные места у атомов углерода присоединились две гидроксильные группы. Формула этилена – С2Н4, после разрыва кранной связи и присоединения гидроксильных групп (через несколько стадий) она выглядит как С2Н4(ОН)2. Это и есть этиленгликоль.
Молекуле этилена присуща линейная структура, в то время как двухатомный спирт имеет некое подобие транс-конфигурции в размещении гидроксильных групп по отношению к углеродному остову и друг к другу (в полной мере этот термин применим к положению относительно кратной связи). Такая дислокация соответствует самому удаленному расположению водородов из функциональных групп, меньшей энергии, а значит – максимальной устойчивости системы. Попросту говоря, одна ОН-группа «смотрит» вверх, а другая — вниз. В то же время неустойчивыми являются соединения с двумя гидроксилами: при одном атоме карбона, образуясь в реакционной смеси, они тут же дегидратируются, переходя в альдегиды.
Классификационная принадлежность
Химические свойства этиленгликоля определяются его происхождением из группы многоатомных спиртов, а именно подгруппы диолов, то есть соединений с двумя гидроксильными фрагментами у соседних атомов карбона. Веществом, также содержащим несколько ОН-заместителей, является и глицерин. Он имеет три спиртовых функциональных группы и является самым распространённым представителем своего подкласса.
Многие соединения этого класса также получают и используют в химическом производстве для различных синтезов и прочих целей, но применение этиленгликоля имеет более серьёзные масштабы и задействовано практически во всех отраслях промышленности. Этот вопрос будет рассмотрен ниже более подробно.
Физические характеристики
Применение этиленгликоля объясняется наличием ряда свойств, которые присущи многоатомным спиртам. Это отличительные черты, характерные только для данного класса органических соединений.
Самое важно из свойств – это неограниченная способность смешиваться с Н2О. Вода + этиленгликоль даёт раствор, обладающий уникальной характеристикой: температура его замерзания, в зависимости от концентрации диола, ниже на 70 градусов, чем у чистого дистиллята. Важно отметить, что зависимость эта нелинейная, и по достижении определённого количественного содержания гликоля начинается обратный эффект – температура замерзания повышается при увеличении процентного содержания растворяемого вещества. Эта особенность нашла применение в области производства различных антифризов, жидкостей «незамерзаек», которые кристаллизуются при крайне низких термических характеристиках окружающей среды.
Кроме как в воде, процесс растворения отлично протекает в спирте и ацетоне, но не наблюдается в парафинах, бензолах, эфирах и тетрахлорметане. В отличие от своего алифатического родоначальника — такого газообразного вещества, как этилен, этиленгликоль – это сиропоподобная,прозрачная, с незначительным желтым оттенком жидкость, сладковатая по вкусу, с нехарактерным запахом, практически нелетучая. Замерзание стопроцентного этиленгликоля происходит при — 12,6 градусах Цельсия, а кипение – при +197,8. В нормальных условиях плотность составляет 1,11 г/см 3 .
Методы получения
Этиленгликоль можно получить несколькими способами, некоторые из них сегодня имеют лишь историческое или препаративное значение, а другие активно используются человеком в промышленных масштабах и не только. Следуя в хронологическом порядке, рассмотрим самые важные.
Выше уже был описан первый метод получения этиленгликоля из дибромэтана. Формула этилена, двойная связь которого разорвана, а свободные валентности заняты галогенами, — главного исходного вещества в данной реакции — помимо углерода и водорода имеет в своём составе два атома брома. Образование промежуточного соединения на первой ступени процесса возможно как раз благодаря их отщеплению, т. е. замещению ацетатными группами, которые при дальнейшем гидролизе превращаются в спиртовые.
В процессе дальнейшего развития науки стало возможным получение этиленгликоля прямым гидролизом любых этанов, замещенных двумя галогенами у соседних атомов карбона, с помощью водных растворов карбонатов металлов из щелочной группы или (менее экологичный реагент) Н2О и диоксида свинца. Реакция довольно «трудоёмкая» и протекает лишь при значительно повышенных температурах и давлении, но это не помешало немцам в периоды мировых войн использовать этот метод для производства этиленгликоля в промышленных масштабах.
Свою роль в становлении органической химии сыграл и способ получения этиленгликоля из этиленхлоргидрина путём его гидролиза угольными солями металлов щелочной группы. При повышении температуры реакции до 170 градусов выход целевого продукта достигал 90 %. Но был значительный недостаток – гликоль нужно было как-то извлекать из раствора соли, что непосредственно сопряжено с рядом трудностей. Учёные решили этот вопрос, разработав метод с тем же исходным веществом, но разбив процесс на две стадии.
Гидролиз этиленгликольацетатов, являясь ранее завершающей стадией метода Вюрца, стал отдельным способом, когда сумели получить исходный реагент окислением этилена в уксусной кислоте кислородом, то есть без применения дорогих и совсем неэкологичных соединений галогенов.
Известно также много способов производства этиленгликоля путём окисления этилена гидроперекисями, перекисями, органическими надкислотами в присутствии катализаторов (соединений осмия), хлоратом калия и др. Также существуют электрохимические и радиационно-химические методы.
Характеристика общих химических свойств
Химические свойства этиленгликоля определяются его функциональными группами. В реакциях может принимать участие один гидроксильный заместитель или оба, в зависимости от условий процесса. Главное отличие в реакционной способности заключается в том, что за счёт наличия у многоатомного спирта нескольких гидроксилов и их взаимного влияния проявляются более сильные кислотные свойства, чем у одноатомных «собратьев». Поэтому в реакциях со щелочами продуктами являются соли (для гликоля – гликоляты, для глицерина – глицераты).
В химические свойства этиленгликоля, равно как и глицерина, входят все реакции спиртов из категории одноатомных. Гликоль даёт полные и неполные эфиры в реакциях с одноосновными кислотами, гликоляты, соответственно, образуются с щелочными металлами, а при химическом процессе с сильными кислотами или их солями выделяется альдегид уксусной кислоты — за счёт отщепления от молекулы атома водорода.
Реакции с активными металлами
Взаимодействие этиленгликоля с активными металлами (стоящими после водорода в химическом ряде напряженности) при повышенных температурах даёт этиленгликолят соответствующего металла, плюс выделяется водород.
Качественная реакция на этиленгликоль
Отличить многоатомный спирт от любой другой жидкости можно с помощью наглядной реакции, характерной только для данного класса соединений. Для этого к бесцветному раствору спирта вливают свежеосажденный гидроксид меди (2), имеющий характерный голубой оттенок. При взаимодействии смешанных компонентов наблюдается растворение осадка и окрашивание раствора в насыщенно синий цвет — в результате образования гликолята меди (2).
Читать еще: Что можно есть при гастроэнтерите?Полимеризация
Химические свойства этиленгликоля имеют большое значение для производства растворителей. Межмолекулярная дегидратация упомянутого вещества, то есть отщепление воды от каждой из двух молекул гликоля и их последующее объединение (одна гидроксильная группа отщепляется полностью, а от другой отходит только водород), даёт возможность получения уникального органического растворителя – диоксана, который часто используется в органической химии, несмотря на его высокую токсичность.
Обмен гидроксила на галоген
При взаимодействии этиленгликоля с галогеноводородными кислотами наблюдается замена гидроксильных групп соответствующим галогеном. Степень замещения зависит от мольной концентрации галогенводорода в реакционной смеси:
Получение эфиров
В реакциях этиленгликоля с азотной кислотой (определённой концентрации) и одноосновными органическими кислотами (муравьиной, уксусной, пропионовой, масленой, валерьяновой и т. д.) происходит образование сложных и, соответственно, простых моноэфиров. При других концентрация азотной кислоты – ди- и тринитроэфиров гликоля. В качестве катализатора используется серная кислота заданной концентрации.
Важнейшие производные этиленгликоля
Ценными веществами, которые можно получить из многоатомных спиртов с помощью несложных химических реакций (описанных выше), являются эфиры этиленгликоля. А именно: монометиловый и моноэтиловый, формулы которых — НО-СН2-СН2-О-СН3 и НО-СН2-СН2-О-С2Н5 соответственно. По химические свойства они во многом похожи на гликоли, но, так же, как и любой другой класс соединений, имеют уникальные реакционные особенности, присущие только им:
- Монометилэтиленгликоль представляет собой жидкость без цвета, но с характерным отвратным запахом, закипающую при 124,6 градусах Цельсия, отлично растворяющуюся в этаноле, других органических растворителях и воде, значительно более летучую, чем гликоль, и с плотностью, меньшей, чем у воды (порядка 0,965 г/см 3 ).
- Диметилэтиленгликоль – также жидкость, но с менее характерным запахом, плотностью 0,935 г/см 3 , температурой закипания 134 градуса выше ноля и растворимостью, сравнительной с предыдущим гомологом.
Применение целлозольвов — так в общем называют моноэфиры этиленгликоля — довольно распространено. Они используются в качестве реагентов и растворителей в органическом синтезе. Также применяются и их физические свойства для антикоррозийных и антикристаллизационных добавок в антифризы и моторные масла.
Области применения и ценовая политика продукционного ряда
Стоимость на заводах и предприятиях, занимающихся производством и продажей подобных реактивов, колеблется в среднем около 100 рублей за килограмм такого химического соединения, как этиленгликоль. Цена зависит от чистоты вещества и максимального процентного содержания целевого продукта.
Применение этиленгликоля не ограничивается какой-то одной областью. Так, в качестве сырья его используют в производстве органических растворителей, искусственных смол и волокон, жидкостей, замерзающих при отрицательных температурах. Он задействован во многих промышленных отраслях, таких как автомобильная, авиационная, фармацевтическая, электротехническая, кожевенная, табачная. Неоспоримо весомо его значение для органического синтеза.
Важно помнить, что гликоль – это токсичное соединение, которое может нанести непоправимый вред здоровью человека. Поэтому его хранят в герметичных сосудах из алюминия или стали с обязательным внутренним слоем, защищающим ёмкость от коррозии, только в вертикальных положениях и помещениях, не снабженных отопительными системами, но с хорошей вентиляцией. Срок – не более пяти лет.
Химические свойства этиленгликоля, характеристика. Двухатомный спирт. Эфиры этиленгликоля
Самые известные и применяемые в жизни человека и в промышленности вещества, принадлежащие к категории многоатомных спиртов – это этиленгликоль и глицерин. Их исследование и использование началось несколько веков назад, но свойства этих органических соединений во многом неповторимы и уникальны, что делает их незаменимыми и по сей день. Многоатомные спирты используют во многих химических синтезах, отраслях промышленности и сферах человеческой жизнедеятельности.
Первое «знакомство» с этиленгликолем и глицерином: история получения
В 1859 году, посредством двухстадийного процесса взаимодействия дибромэтана с ацетатом серебра и последующей обработки едким кали полученного в первой реакции этиленгликольдиацетата, Шарль Вюрц впервые синтезировал этиленгликоль. Некоторое время спустя был разработан метод прямого гидролиза дибромэтана, но в промышленных масштабах в начале двадцатого века двухатомный спирт 1,2-диоксиэтан, он же – моноэтиленгликоль, или просто гликоль, в США получали посредством гидролиза этиленхлоргидрина.
На сегодняшний день и в промышленности, и в лаборатории применяют ряд других методов, новых, более экономичных с сырьевой и энергетической точек зрения, и экологичных, так как применение реагентов, содержащих или выделяющих хлор, токсины, канцерогены и другие опасные для окружающей среды и человека вещества, сокращается по мере развития «зелёной» химии.
Аптекарем Карлом Вильгельмом Шееле в 1779 году был открыт глицерин, а особенности состава соединения изучил в 1836 году Теофиль Жуль Пелуз. Двумя десятилетиями позже было установлено и обосновано строение молекулы данного трёхатомного спирта в трудах Пьера Эжена Марселея Вертело и Шарля Вюрца. Наконец, ещё двадцать лет спустя Шарль Фридель провёл полный синтез глицерина. В настоящее время промышленность использует два метода его получения: через хлористый аллил из пропилена, а также через акролеин. Химические свойства этиленгиликоля, как и глицерина, широко используют в различных сферах химического производства.
Строение и структура соединения
В основе молекулы лежит непредельный углеводородный скелет этилена, состоящий из двух атомов карбона, в котором произошёл разрыв двойной связи. На освободившиеся валентные места у атомов углерода присоединились две гидроксильные группы. Формула этилена – С2Н4, после разрыва кранной связи и присоединения гидроксильных групп (через несколько стадий) она выглядит как С2Н4(ОН)2. Это и есть этиленгликоль.
Молекуле этилена присуща линейная структура, в то время как двухатомный спирт имеет некое подобие транс-конфигурции в размещении гидроксильных групп по отношению к углеродному остову и друг к другу (в полной мере этот термин применим к положению относительно кратной связи). Такая дислокация соответствует самому удаленному расположению водородов из функциональных групп, меньшей энергии, а значит – максимальной устойчивости системы. Попросту говоря, одна ОН-группа «смотрит» вверх, а другая — вниз. В то же время неустойчивыми являются соединения с двумя гидроксилами: при одном атоме карбона, образуясь в реакционной смеси, они тут же дегидратируются, переходя в альдегиды.
Классификационная принадлежность
Химические свойства этиленгликоля определяются его происхождением из группы многоатомных спиртов, а именно подгруппы диолов, то есть соединений с двумя гидроксильными фрагментами у соседних атомов карбона. Веществом, также содержащим несколько ОН-заместителей, является и глицерин. Он имеет три спиртовых функциональных группы и является самым распространённым представителем своего подкласса.
Многие соединения этого класса также получают и используют в химическом производстве для различных синтезов и прочих целей, но применение этиленгликоля имеет более серьёзные масштабы и задействовано практически во всех отраслях промышленности. Этот вопрос будет рассмотрен ниже более подробно.
Физические характеристики
Применение этиленгликоля объясняется наличием ряда свойств, которые присущи многоатомным спиртам. Это отличительные черты, характерные только для данного класса органических соединений.
Самое важно из свойств – это неограниченная способность смешиваться с Н2О. Вода + этиленгликоль даёт раствор, обладающий уникальной характеристикой: температура его замерзания, в зависимости от концентрации диола, ниже на 70 градусов, чем у чистого дистиллята. Важно отметить, что зависимость эта нелинейная, и по достижении определённого количественного содержания гликоля начинается обратный эффект – температура замерзания повышается при увеличении процентного содержания растворяемого вещества. Эта особенность нашла применение в области производства различных антифризов, жидкостей «незамерзаек», которые кристаллизуются при крайне низких термических характеристиках окружающей среды.
Кроме как в воде, процесс растворения отлично протекает в спирте и ацетоне, но не наблюдается в парафинах, бензолах, эфирах и тетрахлорметане. В отличие от своего алифатического родоначальника — такого газообразного вещества, как этилен, этиленгликоль – это сиропоподобная,прозрачная, с незначительным желтым оттенком жидкость, сладковатая по вкусу, с нехарактерным запахом, практически нелетучая. Замерзание стопроцентного этиленгликоля происходит при — 12,6 градусах Цельсия, а кипение – при +197,8. В нормальных условиях плотность составляет 1,11 г/см 3 .
Методы получения
Этиленгликоль можно получить несколькими способами, некоторые из них сегодня имеют лишь историческое или препаративное значение, а другие активно используются человеком в промышленных масштабах и не только. Следуя в хронологическом порядке, рассмотрим самые важные.
Выше уже был описан первый метод получения этиленгликоля из дибромэтана. Формула этилена, двойная связь которого разорвана, а свободные валентности заняты галогенами, — главного исходного вещества в данной реакции — помимо углерода и водорода имеет в своём составе два атома брома. Образование промежуточного соединения на первой ступени процесса возможно как раз благодаря их отщеплению, т. е. замещению ацетатными группами, которые при дальнейшем гидролизе превращаются в спиртовые.
В процессе дальнейшего развития науки стало возможным получение этиленгликоля прямым гидролизом любых этанов, замещенных двумя галогенами у соседних атомов карбона, с помощью водных растворов карбонатов металлов из щелочной группы или (менее экологичный реагент) Н2О и диоксида свинца. Реакция довольно «трудоёмкая» и протекает лишь при значительно повышенных температурах и давлении, но это не помешало немцам в периоды мировых войн использовать этот метод для производства этиленгликоля в промышленных масштабах.
Свою роль в становлении органической химии сыграл и способ получения этиленгликоля из этиленхлоргидрина путём его гидролиза угольными солями металлов щелочной группы. При повышении температуры реакции до 170 градусов выход целевого продукта достигал 90 %. Но был значительный недостаток – гликоль нужно было как-то извлекать из раствора соли, что непосредственно сопряжено с рядом трудностей. Учёные решили этот вопрос, разработав метод с тем же исходным веществом, но разбив процесс на две стадии.
Гидролиз этиленгликольацетатов, являясь ранее завершающей стадией метода Вюрца, стал отдельным способом, когда сумели получить исходный реагент окислением этилена в уксусной кислоте кислородом, то есть без применения дорогих и совсем неэкологичных соединений галогенов.
Читать еще: Признаки, причины и лечение запора у собакИзвестно также много способов производства этиленгликоля путём окисления этилена гидроперекисями, перекисями, органическими надкислотами в присутствии катализаторов (соединений осмия), хлоратом калия и др. Также существуют электрохимические и радиационно-химические методы.
Характеристика общих химических свойств
Химические свойства этиленгликоля определяются его функциональными группами. В реакциях может принимать участие один гидроксильный заместитель или оба, в зависимости от условий процесса. Главное отличие в реакционной способности заключается в том, что за счёт наличия у многоатомного спирта нескольких гидроксилов и их взаимного влияния проявляются более сильные кислотные свойства, чем у одноатомных «собратьев». Поэтому в реакциях со щелочами продуктами являются соли (для гликоля – гликоляты, для глицерина – глицераты).
В химические свойства этиленгликоля, равно как и глицерина, входят все реакции спиртов из категории одноатомных. Гликоль даёт полные и неполные эфиры в реакциях с одноосновными кислотами, гликоляты, соответственно, образуются с щелочными металлами, а при химическом процессе с сильными кислотами или их солями выделяется альдегид уксусной кислоты — за счёт отщепления от молекулы атома водорода.
Реакции с активными металлами
Взаимодействие этиленгликоля с активными металлами (стоящими после водорода в химическом ряде напряженности) при повышенных температурах даёт этиленгликолят соответствующего металла, плюс выделяется водород.
Качественная реакция на этиленгликоль
Отличить многоатомный спирт от любой другой жидкости можно с помощью наглядной реакции, характерной только для данного класса соединений. Для этого к бесцветному раствору спирта вливают свежеосажденный гидроксид меди (2), имеющий характерный голубой оттенок. При взаимодействии смешанных компонентов наблюдается растворение осадка и окрашивание раствора в насыщенно синий цвет — в результате образования гликолята меди (2).
Полимеризация
Химические свойства этиленгликоля имеют большое значение для производства растворителей. Межмолекулярная дегидратация упомянутого вещества, то есть отщепление воды от каждой из двух молекул гликоля и их последующее объединение (одна гидроксильная группа отщепляется полностью, а от другой отходит только водород), даёт возможность получения уникального органического растворителя – диоксана, который часто используется в органической химии, несмотря на его высокую токсичность.
Обмен гидроксила на галоген
При взаимодействии этиленгликоля с галогеноводородными кислотами наблюдается замена гидроксильных групп соответствующим галогеном. Степень замещения зависит от мольной концентрации галогенводорода в реакционной смеси:
Получение эфиров
В реакциях этиленгликоля с азотной кислотой (определённой концентрации) и одноосновными органическими кислотами (муравьиной, уксусной, пропионовой, масленой, валерьяновой и т. д.) происходит образование сложных и, соответственно, простых моноэфиров. При других концентрация азотной кислоты – ди- и тринитроэфиров гликоля. В качестве катализатора используется серная кислота заданной концентрации.
Важнейшие производные этиленгликоля
Ценными веществами, которые можно получить из многоатомных спиртов с помощью несложных химических реакций (описанных выше), являются эфиры этиленгликоля. А именно: монометиловый и моноэтиловый, формулы которых — НО-СН2-СН2-О-СН3 и НО-СН2-СН2-О-С2Н5 соответственно. По химические свойства они во многом похожи на гликоли, но, так же, как и любой другой класс соединений, имеют уникальные реакционные особенности, присущие только им:
- Монометилэтиленгликоль представляет собой жидкость без цвета, но с характерным отвратным запахом, закипающую при 124,6 градусах Цельсия, отлично растворяющуюся в этаноле, других органических растворителях и воде, значительно более летучую, чем гликоль, и с плотностью, меньшей, чем у воды (порядка 0,965 г/см 3 ).
- Диметилэтиленгликоль – также жидкость, но с менее характерным запахом, плотностью 0,935 г/см 3 , температурой закипания 134 градуса выше ноля и растворимостью, сравнительной с предыдущим гомологом.
Применение целлозольвов — так в общем называют моноэфиры этиленгликоля — довольно распространено. Они используются в качестве реагентов и растворителей в органическом синтезе. Также применяются и их физические свойства для антикоррозийных и антикристаллизационных добавок в антифризы и моторные масла.
Области применения и ценовая политика продукционного ряда
Стоимость на заводах и предприятиях, занимающихся производством и продажей подобных реактивов, колеблется в среднем около 100 рублей за килограмм такого химического соединения, как этиленгликоль. Цена зависит от чистоты вещества и максимального процентного содержания целевого продукта.
Применение этиленгликоля не ограничивается какой-то одной областью. Так, в качестве сырья его используют в производстве органических растворителей, искусственных смол и волокон, жидкостей, замерзающих при отрицательных температурах. Он задействован во многих промышленных отраслях, таких как автомобильная, авиационная, фармацевтическая, электротехническая, кожевенная, табачная. Неоспоримо весомо его значение для органического синтеза.
Важно помнить, что гликоль – это токсичное соединение, которое может нанести непоправимый вред здоровью человека. Поэтому его хранят в герметичных сосудах из алюминия или стали с обязательным внутренним слоем, защищающим ёмкость от коррозии, только в вертикальных положениях и помещениях, не снабженных отопительными системами, но с хорошей вентиляцией. Срок – не более пяти лет.
Двухатомные спирты (гликоли).
Двухатомные спирты (гликоли) содержат в молекуле две гидроксильных группы при разных углеродных атомах.
Общая формула этих спиртов CnH2n(OH)2. Первым представителе двухатомных спиртов является этиленгликоль (этандиол) НОСН2—СН2ОН.
Номенклатура. Чтобы назвать эти спирты по систематической номенклатуре, к названию алкана добавляют суффикс -диол, а цифрам указывают место гидроксилов в углеродной цепи:
По рациональной номенклатуре названия двухатомных спиртов можно составить из названий соответствующих алкеновых углеводородов с добавлением слова гликоль:
Изомерия этих спиртов зависит от строения углеродной цепи и расположения в ней двух гидроксильных групп (a-, b-, g-гликоли и т.д.):
Получение. В методах получения двухатомных и одноатомных спиртов много общего. Так, двухатомные спирты можно получать:
1. Гидролизом дигалогенопроизводных:
2. Окислением этиленовых углеводородов:
3. Гидратацией оксида этилена:
Физические свойства. Низшие гликоли (от греч. glykys — сладкий) — сиропообразные, сладкие на вкус, растворимые в воде вещества. Гликоли кипят при более высокой температуре и имеют большую плотность, чем соответствующие им (с тем же числом углеродных атомов) одноатомные спирты. Это объясняется присутствием второй гидроксильной группы, что ведет к образованию дополнительных водородных связей.
Химические свойства. Двухатомные спирты в химических реакциях могут реагировать одной или двумя гидроксильными группами.
1. Образование гликолятов. В отличие от одноатомных спиртов двухатомные легко вступают во взаимодействие не только со щелочными металлами, но и с оксидами и гидроксидами тяжелых металлов. Образующиеся вещества называют гликолятами:
этилен- гликолят меди (комп-
-гликоль лексное соединение)
2. Реакции дегидратации. Эти реакции, как известно, могут быть внутримолекулярными и межмолекулярными:
а) внутримолекулярная дегидратация:
этилен- виниловый уксусный
гликоль спирт альдегид
б) межмолекулярная дегидратация:
-H 2 O диэтилентликоль
В случае (б) процесс может идти и дальше — с образованием полимера:
При межмолекулярной дегидратации образуются не только линейные но и циклические продукты:
Диоксан используют в качестве растворителя (осторожно: токсичен).
3. Образование простых и сложных эфиров. Взаимодействуя спиртами или кислотами (органическими или неорганическими), гликоли образуют простые и сложные эфиры:
4. Замена гидроксильных групп на галоген:
5. Окисление. При окислении двухатомные спирты образуют ряд промежуточных продуктов. Например, при окислении этиленгликоля образуются: гликолевый альдегид (НОСН2—СНО), глиоксаль (ОНС—СНО), гликолевая кислота (НОСН2—СООН), глиоксалевая кислота (ОНС—СООН) и щавелевая кислота (HOOС—COOH). Щавелевая кислота обычно является предпоследним продуктом окисления многих органических соединений.
Дата добавления: 2015-09-29 ; просмотров: 4366 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Химические свойства этиленгликоля, характеристика. Двухатомный спирт. Эфиры этиленгликоля. Общая характеристика: номенклатура и изомерия двухатомных спиртов. Физические и химические свойства
Самые известные и применяемые в жизни человека и в промышленности вещества, принадлежащие к категории многоатомных спиртов — это этиленгликоль и глицерин. Их исследование и использование началось несколько веков назад, но свойства этих во многом неповторимы и уникальны, что делает их незаменимыми и по сей день. Многоатомные спирты используют во многих химических синтезах, отраслях промышленности и сферах человеческой жизнедеятельности.
Первое «знакомство» с этиленгликолем и глицерином: история получения
В 1859 году, посредством двухстадийного процесса взаимодействия дибромэтана с ацетатом серебра и последующей обработки едким кали полученного в первой реакции этиленгликольдиацетата, Шарль Вюрц впервые синтезировал этиленгликоль. Некоторое время спустя был разработан метод прямого гидролиза дибромэтана, но в промышленных масштабах в начале двадцатого века двухатомный спирт 1,2-диоксиэтан, он же — моноэтиленгликоль, или просто гликоль, в США получали посредством гидролиза этиленхлоргидрина.
На сегодняшний день и в промышленности, и в лаборатории применяют ряд других методов, новых, более экономичных с сырьевой и энергетической точек зрения, и экологичных, так как применение реагентов, содержащих или выделяющих хлор, токсины, канцерогены и другие опасные для окружающей среды и человека вещества, сокращается по мере развития «зелёной» химии.
Аптекарем Карлом Вильгельмом Шееле в 1779 году был открыт глицерин, а особенности состава соединения изучил в 1836 году Теофиль Жуль Пелуз. Двумя десятилетиями позже было установлено и обосновано строение молекулы данного трёхатомного спирта в трудах Пьера Эжена Марселея Вертело и Шарля Вюрца. Наконец, ещё двадцать лет спустя Шарль Фридель провёл полный синтез глицерина. В настоящее время промышленность использует два метода его получения: через хлористый аллил из пропилена, а также через акролеин. Химические свойства этиленгиликоля, как и глицерина, широко используют в различных сферах химического производства.
Строение и структура соединения
В основе молекулы лежит непредельный углеводородный скелет этилена, состоящий из двух атомов карбона, в котором произошёл разрыв двойной связи. На освободившиеся валентные места у атомов углерода присоединились две гидроксильные группы. Формула этилена — С 2 Н 4 , после разрыва кранной связи и присоединения гидроксильных групп (через несколько стадий) она выглядит как С 2 Н 4 (ОН) 2 . Это и есть этиленгликоль.
Молекуле этилена присуща линейная структура, в то время как двухатомный спирт имеет некое подобие транс-конфигурции в размещении гидроксильных групп по отношению к углеродному остову и друг к другу (в полной мере этот термин применим к положению относительно кратной связи). Такая дислокация соответствует самому удаленному расположению водородов из функциональных групп, меньшей энергии, а значит — максимальной устойчивости системы. Попросту говоря, одна ОН-группа «смотрит» вверх, а другая — вниз. В то же время неустойчивыми являются соединения с двумя гидроксилами: при одном атоме карбона, образуясь в реакционной смеси, они тут же дегидратируются, переходя в альдегиды.
Читать еще: Симптомы и лечение сальмонеллеза у взрослыхКлассификационная принадлежность
Химические свойства этиленгликоля определяются его происхождением из группы многоатомных спиртов, а именно подгруппы диолов, то есть соединений с двумя гидроксильными фрагментами у соседних атомов карбона. Веществом, также содержащим несколько ОН-заместителей, является и глицерин. Он имеет три спиртовых функциональных группы и является самым распространённым представителем своего подкласса.
Многие соединения этого класса также получают и используют в химическом производстве для различных синтезов и прочих целей, но применение этиленгликоля имеет более серьёзные масштабы и задействовано практически во всех отраслях промышленности. Этот вопрос будет рассмотрен ниже более подробно.
Физические характеристики
Применение этиленгликоля объясняется наличием ряда свойств, которые присущи многоатомным спиртам. Это отличительные черты, характерные только для данного класса органических соединений.
Самое важно из свойств — это неограниченная способность смешиваться с Н 2 О. Вода + этиленгликоль даёт раствор, обладающий уникальной характеристикой: температура его замерзания, в зависимости от концентрации диола, ниже на 70 градусов, чем у чистого дистиллята. Важно отметить, что зависимость эта нелинейная, и по достижении определённого количественного содержания гликоля начинается обратный эффект — температура замерзания повышается при увеличении процентного содержания растворяемого вещества. Эта особенность нашла применение в области производства различных антифризов, жидкостей «незамерзаек», которые кристаллизуются при крайне низких термических характеристиках окружающей среды.
Кроме как в воде, процесс растворения отлично протекает в спирте и ацетоне, но не наблюдается в парафинах, бензолах, эфирах и тетрахлорметане. В отличие от своего алифатического родоначальника — такого газообразного вещества, как этилен, этиленгликоль — это сиропоподобная,прозрачная, с незначительным желтым оттенком жидкость, сладковатая по вкусу, с нехарактерным запахом, практически нелетучая. Замерзание стопроцентного этиленгликоля происходит при — 12,6 градусах Цельсия, а кипение — при +197,8. В нормальных условиях плотность составляет 1,11 г/см 3 .
Методы получения
Этиленгликоль можно получить несколькими способами, некоторые из них сегодня имеют лишь историческое или препаративное значение, а другие активно используются человеком в промышленных масштабах и не только. Следуя в хронологическом порядке, рассмотрим самые важные.
Выше уже был описан первый метод получения этиленгликоля из дибромэтана. Формула этилена, двойная связь которого разорвана, а свободные валентности заняты галогенами, — главного исходного вещества в данной реакции — помимо углерода и водорода имеет в своём составе два атома брома. Образование промежуточного соединения на первой ступени процесса возможно как раз благодаря их отщеплению, т. е. замещению ацетатными группами, которые при дальнейшем гидролизе превращаются в спиртовые.
В процессе дальнейшего развития науки стало возможным получение этиленгликоля прямым гидролизом любых этанов, замещенных двумя галогенами у соседних атомов карбона, с помощью водных растворов карбонатов металлов из щелочной группы или (менее экологичный реагент) Н 2 О и диоксида свинца. Реакция довольно «трудоёмкая» и протекает лишь при значительно повышенных температурах и давлении, но это не помешало немцам в периоды мировых войн использовать этот метод для производства этиленгликоля в промышленных масштабах.
Свою роль в становлении органической химии сыграл и способ получения этиленгликоля из этиленхлоргидрина путём его гидролиза угольными солями металлов щелочной группы. При повышении температуры реакции до 170 градусов выход целевого продукта достигал 90 %. Но был значительный недостаток — гликоль нужно было как-то извлекать из раствора соли, что непосредственно сопряжено с рядом трудностей. Учёные решили этот вопрос, разработав метод с тем же исходным веществом, но разбив процесс на две стадии.
Гидролиз этиленгликольацетатов, являясь ранее завершающей стадией метода Вюрца, стал отдельным способом, когда сумели получить исходный реагент окислением этилена в уксусной кислоте кислородом, то есть без применения дорогих и совсем неэкологичных соединений галогенов.
Известно также много способов производства этиленгликоля путём окисления этилена гидроперекисями, перекисями, органическими надкислотами в присутствии катализаторов (соединений осмия), и др. Также существуют электрохимические и радиационно-химические методы.
Характеристика общих химических свойств
Химические свойства этиленгликоля определяются его функциональными группами. В реакциях может принимать участие один гидроксильный заместитель или оба, в зависимости от условий процесса. Главное отличие в реакционной способности заключается в том, что за счёт наличия у многоатомного спирта нескольких гидроксилов и их взаимного влияния проявляются более сильные чем у одноатомных «собратьев». Поэтому в реакциях со щелочами продуктами являются соли (для гликоля — гликоляты, для глицерина — глицераты).
В химические свойства этиленгликоля, равно как и глицерина, входят все реакции спиртов из категории одноатомных. Гликоль даёт полные и неполные эфиры в реакциях с одноосновными кислотами, гликоляты, соответственно, образуются с щелочными металлами, а при химическом процессе с сильными кислотами или их солями выделяется альдегид уксусной кислоты — за счёт отщепления от молекулы атома водорода.
Реакции с активными металлами
Взаимодействие этиленгликоля с активными металлами (стоящими после водорода в химическом ряде напряженности) при повышенных температурах даёт этиленгликолят соответствующего металла, плюс выделяется водород.
С 2 Н 4 (ОН) 2 + Х → С 2 Н 4 О 2 Х, где Х — активный двухвалентный металл.
на этиленгликоль
Отличить многоатомный спирт от любой другой жидкости можно с помощью наглядной реакции, характерной только для данного класса соединений. Для этого к бесцветному раствору спирта вливают свежеосажденный (2), имеющий характерный голубой оттенок. При взаимодействии смешанных компонентов наблюдается растворение осадка и окрашивание раствора в насыщенно синий цвет — в результате образования гликолята меди (2).
Полимеризация
Химические свойства этиленгликоля имеют большое значение для производства растворителей. Межмолекулярная дегидратация упомянутого вещества, то есть отщепление воды от каждой из двух молекул гликоля и их последующее объединение (одна гидроксильная группа отщепляется полностью, а от другой отходит только водород), даёт возможность получения уникального органического растворителя — диоксана, который часто используется в органической химии, несмотря на его высокую токсичность.
Обмен гидроксила на галоген
При взаимодействии этиленгликоля с галогеноводородными кислотами наблюдается замена гидроксильных групп соответствующим галогеном. Степень замещения зависит от мольной концентрации галогенводорода в реакционной смеси:
НО-СН 2 -СН 2 -ОН + 2НХ → Х-СН 2 -СН 2 -Х, где Х — хлор или бром.
Получение эфиров
В реакциях этиленгликоля с азотной кислотой (определённой концентрации) и одноосновными органическими кислотами (муравьиной, уксусной, пропионовой, масленой, валерьяновой и т. д.) происходит образование сложных и, соответственно, простых моноэфиров. При других концентрация азотной кислоты — ди- и тринитроэфиров гликоля. В качестве катализатора используется серная кислота заданной концентрации.
Важнейшие производные этиленгликоля
Ценными веществами, которые можно получить из многоатомных спиртов с помощью несложных (описанных выше), являются эфиры этиленгликоля. А именно: монометиловый и моноэтиловый, формулы которых — НО-СН 2 -СН 2 -О-СН 3 и НО-СН 2 -СН 2 -О-С 2 Н 5 соответственно. По химические свойства они во многом похожи на гликоли, но, так же, как и любой другой класс соединений, имеют уникальные реакционные особенности, присущие только им:
- Монометилэтиленгликоль представляет собой жидкость без цвета, но с характерным отвратным запахом, закипающую при 124,6 градусах Цельсия, отлично растворяющуюся в этаноле, других органических растворителях и воде, значительно более летучую, чем гликоль, и с плотностью, меньшей, чем у воды (порядка 0,965 г/см 3).
- Диметилэтиленгликоль — также жидкость, но с менее характерным запахом, плотностью 0,935 г/см 3 , температурой закипания 134 градуса выше ноля и растворимостью, сравнительной с предыдущим гомологом.
Применение целлозольвов — так в общем называют моноэфиры этиленгликоля — довольно распространено. Они используются в качестве реагентов и растворителей в органическом синтезе. Также применяются и их для антикоррозийных и антикристаллизационных добавок в антифризы и моторные масла.
Области применения и ценовая политика продукционного ряда
Стоимость на заводах и предприятиях, занимающихся производством и продажей подобных реактивов, колеблется в среднем около 100 рублей за килограмм такого химического соединения, как этиленгликоль. Цена зависит от чистоты вещества и максимального процентного содержания целевого продукта.
Применение этиленгликоля не ограничивается какой-то одной областью. Так, в качестве сырья его используют в производстве органических растворителей, искусственных смол и волокон, жидкостей, замерзающих при отрицательных температурах. Он задействован во многих промышленных отраслях, таких как автомобильная, авиационная, фармацевтическая, электротехническая, кожевенная, табачная. Неоспоримо весомо его значение для органического синтеза.
Важно помнить, что гликоль — это токсичное соединение, которое может нанести непоправимый вред здоровью человека. Поэтому его хранят в герметичных сосудах из алюминия или стали с обязательным внутренним слоем, защищающим ёмкость от коррозии, только в вертикальных положениях и помещениях, не снабженных отопительными системами, но с хорошей вентиляцией. Срок — не более пяти лет.
Спирты, молекулы которых содержат две гидроксильные группы, называют двухатомными или гликолями. Общая формула двухатомных спиртов C n H 2n (OH) 2 . Двухатомные спирты образуют гомологический ряд, который можно легко написать, используя гомологический ряд насыщенных углеводородов, заменяя в их молекуле два атома водорода на гидроксильные группы.
Первым и наиболее важным представителем двухатомных спиртов является этиленгликоль НОСН 2 -СН 2 ОН (Т кип. =197 о С). Из него изготовляют антифриз.
Устойчивыми являются гликоли, в молекулах которых гидроксильные группы расположены возле разных углеродных атомов. Если две гидроксильные группы находятся возле одного углеродного атома, то такие двухатомные спирты неустойчивы, легко разлагаются, отщепляя за счет гидроксильных групп воду и превращаются в альдегиды или кетоны:
Можно ли пить при отравлении кефир и насколько он эффективен? Можно ли при отравлении пить кефир Пытаясь помочь организму избавиться от последствий,...
16 05 2024 9:17:32
Больничный лист при цистите: листок нетрудоспособности Дают ли больничный с циститом у женщин Одна из самых распространенных инфекций нижних мочевых путей...
15 05 2024 16:48:30
 Расстройство личности 10 видов расстройств личности и их внешние проявления Расстройствами личности (иначе – конституциональными психопатиями) страдает...
Расстройство личности 10 видов расстройств личности и их внешние проявления Расстройствами личности (иначе – конституциональными психопатиями) страдает...
14 05 2024 8:32:39
 Дизентерия: симптомы и лечение Дизентерия Общие сведения Дизентерия — это инфекционная болезнь общего характера, которую вызывают дизентерийные бактерии....
Дизентерия: симптомы и лечение Дизентерия Общие сведения Дизентерия — это инфекционная болезнь общего характера, которую вызывают дизентерийные бактерии....
13 05 2024 23:33:51
Как закрыть шкаф купе и ящики от маленьких детей своими руками? Как закрыть шкаф купе и ящики от маленьких детей своими руками? Казалось еще только вчера...
12 05 2024 19:20:42
Выделения при беременности Выделения при беременности У беременной женщины волнение может возникать даже по сущему пустяку: то в боку закололо, то...
11 05 2024 21:15:16
 Рак простаты. Причины, симптомы, стадии, лечение заболевания. Операция при раке простаты. Рак предстательной железы Рак простаты — онкологическое...
Рак простаты. Причины, симптомы, стадии, лечение заболевания. Операция при раке простаты. Рак предстательной железы Рак простаты — онкологическое...
10 05 2024 6:55:57
Что такое биологически активные добавки к пище, группы, их действие БАДы – биологически активные добавки Биодобавки – это комплекс из натуральных...
09 05 2024 10:59:13
Кардиалгия и месячные: существует ли взаимосвязь? Кардиалгия Общие сведения Кардиалгия — это болевой синдром сердечного происхождения. Боль не всегда...
08 05 2024 7:38:48
Лечение кифоза грудного отдела позвоночника Кифоз грудного отдела позвоночника - как лечить. Упражнения при лечении кифоза грудного отдела позвоночника...
07 05 2024 19:29:55
 Карбамазепин (финлепсин, тегретол) как нормотимик и препарат для лечения невралгии: отзыв и опыт применения Карбамазепин (финлепсин, тегретол) как...
Карбамазепин (финлепсин, тегретол) как нормотимик и препарат для лечения невралгии: отзыв и опыт применения Карбамазепин (финлепсин, тегретол) как...
06 05 2024 20:43:25
Можно ли новорожденному смотреть телевизор Можно или нельзя грудным детям смотреть телевизор и почему Как только в наши дома проник чудесный прибор с...
05 05 2024 13:31:55
Лечение медом поджелудочной железы — все о терапии панкреатита Употребление меда при панкреатите: можно или нет, как продукт влияет на поджелудочную...
04 05 2024 19:54:25
СМ-Клиника на ул. Лесная (м. Белорусская) «СМ-Клиника» на ул. Лесная (м. «Белорусская») Адрес : ул. Лесная, д. 57, стр. 1 (м. «Белорусская»)....
03 05 2024 0:51:33
 Что делать, если появилась диарея и ломота в теле? Кишечный (желудочный) грипп — температура, рвота, понос Вчера я впервые в жизни одновременно срал и...
Что делать, если появилась диарея и ломота в теле? Кишечный (желудочный) грипп — температура, рвота, понос Вчера я впервые в жизни одновременно срал и...
02 05 2024 10:36:21
Описторхоз: симптомы, лечение, диагностика и профилактика Симптомы и лечение описторхоза у взрослых В этой статье рассмотрим такое заболевание, как...
01 05 2024 0:56:27
 Можно ли пить квас во время беременности? Квас во время беременности – можно ли пить черный или белый и какие требования к продукту во время 1, 2 и 3...
Можно ли пить квас во время беременности? Квас во время беременности – можно ли пить черный или белый и какие требования к продукту во время 1, 2 и 3...
30 04 2024 2:59:59
 Почему повышается холестерин при беременности и как его снизить Повышен холестерин при беременности На протяжении беременности женщина несколько раз сдает...
Почему повышается холестерин при беременности и как его снизить Повышен холестерин при беременности На протяжении беременности женщина несколько раз сдает...
29 04 2024 8:40:55
Стрептококк. Обнаружен стрептококк в носу, горле, зеве, на коже, что делать? Стрептококк у грудных детей. Как выявить лечить инфекцию? Стрептококк у...
28 04 2024 1:39:54
 Первая прогулка со щенком, как она выглядит Первая прогулка щенка на улице: что нужно учесть Выгул собаки – ответственное и в тоже время приятное...
Первая прогулка со щенком, как она выглядит Первая прогулка щенка на улице: что нужно учесть Выгул собаки – ответственное и в тоже время приятное...
27 04 2024 21:54:27
 Ротавирусная инфекция (кишечный грипп) Отличие ротавирусной инфекции от кишечной инфекции. Многие родители паникуют, путая ротавирус, дизентерию и...
Ротавирусная инфекция (кишечный грипп) Отличие ротавирусной инфекции от кишечной инфекции. Многие родители паникуют, путая ротавирус, дизентерию и...
26 04 2024 4:57:21
Что можно приготовить из батата: пять вкусных рецептов для семейного меню Как приготовить батат: 5 простых и вкусных рецептов Батат, также известный как...
25 04 2024 8:23:22
Как лечить воспаление поджелудочной железы в домашних условиях Как лечить панкреатит в домашних условиях быстро и эффективно На сегодняшний день, каждый...
24 04 2024 20:21:16
Фиброз грудной клетки: характеристики и методы лечения Локальный фиброз молочных желез что это такое Причины развития и лечение фиброза грудных желез...
23 04 2024 22:46:22
Лечение рака костей народными средствами Лечение рака костей Рак костей – это злокачественные новообразования, которые поражают костную ткань и...
22 04 2024 14:31:19
 Очень сильно болит желудок: первая помощь Очень сильно болит желудок: первая помощь Боли в желудке бывают различного характера, зависят от причин их...
Очень сильно болит желудок: первая помощь Очень сильно болит желудок: первая помощь Боли в желудке бывают различного характера, зависят от причин их...
21 04 2024 10:24:47
 Дегтярный шампунь от перхоти, польза и вред Дегтярный шампунь от перхоти, польза и вред Березовый деготь – известное средство борьбы с кожными...
Дегтярный шампунь от перхоти, польза и вред Дегтярный шампунь от перхоти, польза и вред Березовый деготь – известное средство борьбы с кожными...
20 04 2024 16:22:53
Сколько Нимесила можно выпить в сутки? Как принимать Нимесил? Нимесил – это противовоспалительное средство категории НПВС, является селективным...
19 04 2024 4:21:44
 Можно ли потолстеть от дыни Можно ли поправиться от дыни? Современные женщины стремятся ухаживать за собой, следить за собственным весом и фигурой и чтобы...
Можно ли потолстеть от дыни Можно ли поправиться от дыни? Современные женщины стремятся ухаживать за собой, следить за собственным весом и фигурой и чтобы...
18 04 2024 0:43:18
 Как снять белый налет с миндалин при ангине Налет на миндалинах 10 октября 2018, 20:31 Эксперт статьи: Курбанов Курбан Саматович 0 28,348 Гланды в полости...
Как снять белый налет с миндалин при ангине Налет на миндалинах 10 октября 2018, 20:31 Эксперт статьи: Курбанов Курбан Саматович 0 28,348 Гланды в полости...
17 04 2024 20:39:14
 Защитить ребёнка от инфекций Инфанриксом Гекса ИНФАНРИКС ГЕКСА Инфанрикс Гекса (Infanrix Hexa) – импортный аналог отечественной прививки против дифтерии,...
Защитить ребёнка от инфекций Инфанриксом Гекса ИНФАНРИКС ГЕКСА Инфанрикс Гекса (Infanrix Hexa) – импортный аналог отечественной прививки против дифтерии,...
16 04 2024 12:55:13
Чистотел при лишае Чистотел при лишае Народная медицина знает много способов как лечить лишай у человека чистотелом. Это лекарственное растение получило...
15 04 2024 9:39:48
Когда и на каком сроке начинает расти живот при беременности На какой неделе беременности начинает расти живот и на каком месяце он сильно заметен?...
14 04 2024 0:38:55
Отличительные признаки строения гермафродитной проглоттиды Отличительные признаки строения гермафродитной проглоттиды Проглоттида представляет собой...
13 04 2024 9:23:32
Что такое ППА? (Прерванный половой акт) Чем вреден прерванный половой акт? Прерванный половой акт (coitus interruptus) — один из древнейших методов...
12 04 2024 18:23:35
Аритмия сердца опасна ли для жизни Что такое аритмия и чем она опасна? Привычнее сравнивать сердце с мотором, хотя по сути оно — самый настоящий насос, за...
11 04 2024 12:43:10
 Повреждения (травмы) глаз (I) Травма глаза. Лечение Ардамакова Алеся Валерьевна Врач-офтальмолог, лазерный хирург Кандидат медицинских наук Глаза...
Повреждения (травмы) глаз (I) Травма глаза. Лечение Ардамакова Алеся Валерьевна Врач-офтальмолог, лазерный хирург Кандидат медицинских наук Глаза...
10 04 2024 9:28:13
Нарушение речи при инсульте — типы отклонений Нарушение речи при инсульте — типы отклонений В результате инсульта происходит нарушение кровообращения в...
09 04 2024 17:10:51
E252 Нитрат калия E252 Нитрат калия Нитрат калия (Potassium nitrate, saltpetre, saltpeter, nitrate of potash, калиевая селитра, E252) Нитратом калия...
08 04 2024 6:15:31
Польза веганства (строгое вегетарианство) лженаучна Польза вегетарианства. Что об этом надо знать? Если вы питаетесь правильно, то лекарства вам не нужны,...
07 04 2024 13:52:32
Древние методы аюрведы для очистки организма от паразитов и глистов Аюрведа против паразитов: лучшие средства, чтобы избавиться от глистов Аюрведа —...
06 04 2024 21:50:59
 Как убрать жировик в домашних условиях? Два способа как удалить жировик в домашних условиях Жировик (липома) – явление крайне неприятное, особенно если...
Как убрать жировик в домашних условиях? Два способа как удалить жировик в домашних условиях Жировик (липома) – явление крайне неприятное, особенно если...
05 04 2024 12:50:59
 Можно ли употреблять капусту больному холециститом? Диета при холецистите Эффективность: лечебный эффект через 14 дней Сроки: от 3 месяцев и более...
Можно ли употреблять капусту больному холециститом? Диета при холецистите Эффективность: лечебный эффект через 14 дней Сроки: от 3 месяцев и более...
04 04 2024 10:17:50
Рак простаты: симптомы, степени, стадии и лечение Симптомы рака предстательной железы по стадиям Ежегодно растет доля рака простаты в общем объеме...
03 04 2024 3:30:47
Вероятность самостоятельных родов после операции кесарево сечение Какими могут быть роды после кесарева сечения Кесарево сечение при первых родах не...
02 04 2024 18:37:22
 Сироп Флавамед при сухом кашле: инструкция по применению препарата В составе одной таблетки препарата содержится 30 мг гидрохлорида амброксола +...
Сироп Флавамед при сухом кашле: инструкция по применению препарата В составе одной таблетки препарата содержится 30 мг гидрохлорида амброксола +...
01 04 2024 7:50:14
 Регулятор артериального давления Берлиприл: инструкция по применению, цена, аналоги и отзывы В состав одной таблетки входит действующее вещество...
Регулятор артериального давления Берлиприл: инструкция по применению, цена, аналоги и отзывы В состав одной таблетки входит действующее вещество...
31 03 2024 10:28:14
ОЗОН Озон в Москве На официальном сайте в каталоге магазина Озон в Москве цены на товары по акции ноябрь 2019 года представлены уже с действующими...
30 03 2024 8:41:26
Лечебная диета №5 Лечебная диета №5 В ХХ веке в России профессор гастроэнтеролог Мануил Певзнер изучал влияние рациона питания человека для облегчения...
29 03 2024 7:12:13
Левомицетин мазь: инструкция по применению, цены, обзор аналогов и отзывы Левомицетин (глазные капли): цена, инструкция по применению, отзывы, аналоги...
28 03 2024 13:30:52
Еще:
здоровье и качество жизни -1 :: здоровье и качество жизни -2 :: здоровье и качество жизни -3 :: здоровье и качество жизни -4 ::


 Как избежать сальмонеллёза: профилактика и причины заражения
Как избежать сальмонеллёза: профилактика и причины заражения 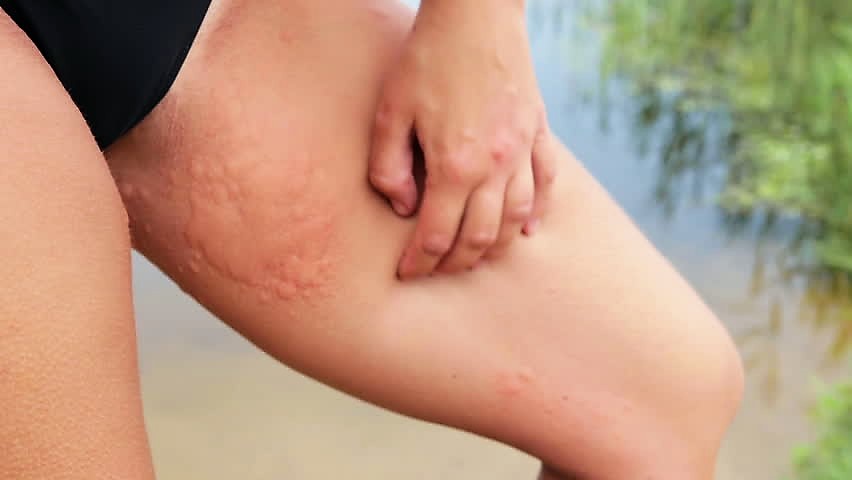 Волдыри на коже: виды и причины образования
Волдыри на коже: виды и причины образования  Нежирные сорта рыбы для диеты и способы ее приготовления
Нежирные сорта рыбы для диеты и способы ее приготовления  Подробно о том, как мыть шпица
Подробно о том, как мыть шпица  16 неделя беременности
16 неделя беременности  Укрепление коротких и длинных ногтей гелем — полезные советы
Укрепление коротких и длинных ногтей гелем — полезные советы  Лечебный шампунь от перхоти в аптеке: рейтинг лучших средств по отзывам покупателей
Лечебный шампунь от перхоти в аптеке: рейтинг лучших средств по отзывам покупателей  Программы и схемы оздоровления компании "Сибирское здоровье"
Программы и схемы оздоровления компании "Сибирское здоровье"  Одинокая женщина желает родить: все методики искусственного оплодотворения
Одинокая женщина желает родить: все методики искусственного оплодотворения  Иммуносупрессоры
Иммуносупрессоры  Выделения в первом триместре
Выделения в первом триместре  Лечебная диета № 5, при заболеваниях печени и желчного пузыря
Лечебная диета № 5, при заболеваниях печени и желчного пузыря  Список транквилизаторов, которые продают без рецептов врачей
Список транквилизаторов, которые продают без рецептов врачей  Симптоматика и лечение ангиодистонии
Симптоматика и лечение ангиодистонии  Обморок и потеря сознания: в чем разница? Как помочь человеку в бессознательном состоянии?
Обморок и потеря сознания: в чем разница? Как помочь человеку в бессознательном состоянии? 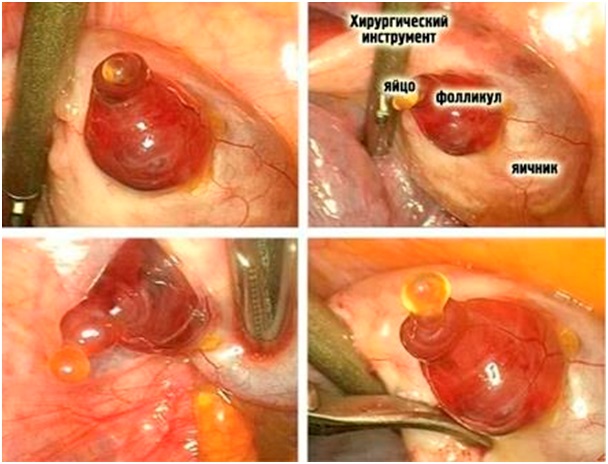 Как узнать, произошло ли зачатие после овуляции — первые признаки беременности
Как узнать, произошло ли зачатие после овуляции — первые признаки беременности  Лечебная физкультура при спондилоартрозе
Лечебная физкультура при спондилоартрозе  Какие тренажеры лучше использовать при сколиозе
Какие тренажеры лучше использовать при сколиозе  СМ-Клиника - Красногвардейский район
СМ-Клиника - Красногвардейский район  Как едят краба: уроки этикета
Как едят краба: уроки этикета  Как едят краба: уроки этикета
Как едят краба: уроки этикета  Что делать, если потеет попа — гипергидроз ануса
Что делать, если потеет попа — гипергидроз ануса  Как поможет ЛФК для восстановления коленных суставов при артрозе 1 и 2 степени?
Как поможет ЛФК для восстановления коленных суставов при артрозе 1 и 2 степени?  10 ранних признаков многоплодной беременности
10 ранних признаков многоплодной беременности  Список продуктов для гипоаллергенной диеты
Список продуктов для гипоаллергенной диеты  СОЭ у женщин — норма в анализе крови и причины повышения (+ таблица)
СОЭ у женщин — норма в анализе крови и причины повышения (+ таблица)  Измерение размера таза у беременных (норма для естественных родов)
Измерение размера таза у беременных (норма для естественных родов)  Когда опускается живот при беременности?
Когда опускается живот при беременности?  Как понять по ощущениям, что подсадка эмбриона прошла успешно
Как понять по ощущениям, что подсадка эмбриона прошла успешно  Можно ли ездить на велосипеде во время беременности?
Можно ли ездить на велосипеде во время беременности?  Высокий эстрадиол у женщин — признаки и методы нормализации гормона
Высокий эстрадиол у женщин — признаки и методы нормализации гормона  Продукты, сжигающие жир на животе и боках, правила питания
Продукты, сжигающие жир на животе и боках, правила питания  Работа палатной медицинской сестры высшей категории
Работа палатной медицинской сестры высшей категории  В каком возрасте можно начинать целоваться
В каком возрасте можно начинать целоваться  Диета и рекомендованный режим питания при долихосигме
Диета и рекомендованный режим питания при долихосигме  Способы повышения уровня прогестерона
Способы повышения уровня прогестерона  Особенности забора стволовых клеток у донора и последствия после процедуры
Особенности забора стволовых клеток у донора и последствия после процедуры  Подробно о вирусе герпеса 6 типа
Подробно о вирусе герпеса 6 типа  Как разработать после перелома лучевой кости руку в домашних условиях
Как разработать после перелома лучевой кости руку в домашних условиях  Диета при сахарном диабете 2 типа: таблица продуктов
Диета при сахарном диабете 2 типа: таблица продуктов  Иммунодепрессанты: классификация и описание
Иммунодепрессанты: классификация и описание  Воспаление околоушного лимфоузла
Воспаление околоушного лимфоузла  Сравниваем и выбираем: Вермокс, Декарис, Пирантел, Немозол, Вормил?
Сравниваем и выбираем: Вермокс, Декарис, Пирантел, Немозол, Вормил?  Опасна ли доброкачественная опухоль в голове
Опасна ли доброкачественная опухоль в голове  Беременность при поздней овуляции особенности течения
Беременность при поздней овуляции особенности течения  Пубертатный период у мальчиков — основные признаки
Пубертатный период у мальчиков — основные признаки  Питание в третьем триместре
Питание в третьем триместре  Чем опасен гиперкератоз плоского эпителия шейки матки
Чем опасен гиперкератоз плоского эпителия шейки матки  Дыня для кормящей мамы
Дыня для кормящей мамы  Гормонотерапия при раке молочной железы
Гормонотерапия при раке молочной железы  Если роды задерживаются
Если роды задерживаются  Таблица правильного питания на каждый день, принципы и особенности его организации
Таблица правильного питания на каждый день, принципы и особенности его организации  Узнаем, как отличить ротавирус от отравления?
Узнаем, как отличить ротавирус от отравления?  Смешанная флора в мазке: что это такое расшифровка
Смешанная флора в мазке: что это такое расшифровка  Сокращаем матку после родов: рекомендации для мам по приведению матки в тонус после беременности
Сокращаем матку после родов: рекомендации для мам по приведению матки в тонус после беременности  Какие упражнения нужно делать при коксартрозе тазобедренного сустава
Какие упражнения нужно делать при коксартрозе тазобедренного сустава  Лечебная диета при артрозе коленного сустава
Лечебная диета при артрозе коленного сустава  Особенности жизни после удаления желчного пузыря
Особенности жизни после удаления желчного пузыря  Почему возникает тошнота и рвота при гастрите и как с ней бороться
Почему возникает тошнота и рвота при гастрите и как с ней бороться  Недоношенные дети: выхаживание и вскармливание в первые дни жизни
Недоношенные дети: выхаживание и вскармливание в первые дни жизни  Нарушение венозного оттока головного мозга
Нарушение венозного оттока головного мозга  ПЭП у новорожденных
ПЭП у новорожденных  Монодиета на 10 дней
Монодиета на 10 дней  Монодиета на 10 дней
Монодиета на 10 дней  Самые распространенные инфекции глаз
Самые распространенные инфекции глаз  Что делать взрослому, если его укусила собака: отвечаем на популярные вопросы
Что делать взрослому, если его укусила собака: отвечаем на популярные вопросы